Au cours de la dernière décennie, les implants dentaires ont été largement utilisés comme base pour les restaurations amovibles ou permanentes chez les patients partiellement ou complètement édentés.
Cette tendance est le résultat des taux de réussite élevés des implants et de la reconstruction supportée par implants. 1,2 Avec l'augmentation de l'utilisation des implants, nous assistons à l'émergence de
de nouvelles maladies inflammatoires – la péri-implantite et la mucite péri-implantaire. Le terme « péri-implantite » a été décrit pour la première fois en 1987 dans un article de Mombelli et al.3.
La maladie a été définie comme une maladie inflammatoire présentant des caractéristiques similaires à celles de la parodontite. Depuis lors, elle a tendance à être considérée comme une entité distincte de la parodontite.
Alors que la mucite péri-implantaire est définie comme une maladie inflammatoire limitée aux tissus mous autour de l'implant, la péri-implantite implique également l'os environnant 4,5.
Diverses études ont présenté différents paramètres cliniques et radiographiques pour définir la mucite péri-implantaire et la péri-implantite, et il existe un manque de critères uniformes et précis.
Pour le diagnostic de chacun de ces diagnostics 6-10.
La définition actuellement acceptée de la péri-implantite selon le huitième consensus de l'EFP comprend un changement de la hauteur de l'os crestal autour de l'implant, la présence de saignement au contact de l'implant et
Sondage et/ou écoulement purulent avec ou sans approfondissement de la poche péri-implantaire11. La littérature présente des rapports variés concernant l'incidence de la mucite péri-implantaire et de la péri-implantite.
En général, l’incidence de la péri-implantite sur 5 à 10 ans est estimée à 101 % des implants et 201 % des patients.12-13
L’incidence de la mucite péri-implantaire est plus élevée – Atieh et ses collègues ont signalé une prévalence de la mucite péri-implantaire chez 63,41 % des patients.
Dans la même étude, en considérant l'implant comme unité statistique, une mucite péri-implantaire a été constatée chez 30,71 % des patients. La forte variabilité dans la déclaration de l'incidence de la péri-implantite
Peut être le résultat d'une définition différente de la maladie (seuil différent de perte osseuse, différences dans la définition de la présence de paramètres inflammatoires – BOP, PD et leur combinaison)
et/ou des durées de suivi différentes. De plus, la population étudiée diffère selon les études.
Étiologie
Les maladies péri-implantaires sont causées en réponse à la présence de bactéries péri-pathogènes sur la surface de l'implant, de manière similaire à leur colonisation sur la surface de la dent.
Leur accumulation entraîne la stimulation et l’activation de médiateurs inflammatoires faisant partie du système immunitaire du patient, ce qui provoque une réaction qui détruit les tissus de fixation de l’implant15.
Le processus inflammatoire de la mucite péri-implantaire est similaire à celui qui se produit autour des dents lors d'une gingivite. La structure de la barrière épithéliale autour des dents et des implants
(L'épithélium de jonction et l'épithélium barrière, respectivement) sont similaires, bien que leurs origines développementales soient différentes. Le tissu conjonctif, contrairement à l'épithélium,
Sa structure et sa composition diffèrent selon qu'il s'agit des gencives autour des dents ou de la muqueuse autour des implants. Autour des implants, la muqueuse contient davantage de collagène et moins de fibroblastes et de vaisseaux sanguins.
Cela peut entraîner une progression plus rapide de la maladie. Contrairement aux dents, les implants présentent différents types de surfaces.
Les surfaces rugueuses présentent apparemment un risque plus élevé de développer une péri-implantite par rapport aux surfaces lisses, dès leur exposition à la cavité buccale.
Cependant, aucune différence n’a été trouvée dans le processus inflammatoire entre les différentes surfaces6.
Facteurs de risque
Il existe plusieurs facteurs de risque pour le développement et la progression de la péri-implantite, notamment une mauvaise hygiène bucco-dentaire16, des résidus de ciment ou d’autres facteurs locaux17,18.
Antécédents de maladie parodontale19-22, tabagisme19,24,25, facteurs génétiques26, diabète et charge occlusale27. Une mauvaise hygiène bucco-dentaire est la principale cause du développement de la maladie péri-implantaire.
(Augmente le risque de péri-implantite de 14,3 fois). L'anatomie de l'implant et de sa restauration ont une influence décisive sur la capacité du patient à éliminer la plaque dentaire de manière optimale.
et peut constituer un facteur de risque pour le développement de la maladie.12,16 De plus, la mobilité des pièces de restauration, qui peut indiquer un desserrage de la vis de structure ou de la couronne elle-même, peut affecter
L'inflammation autour de l'implant, due à l'absence de connexion entre l'implant et les éléments de la restauration, constitue un site potentiel de colonisation bactérienne. De plus, les résidus de ciment sous-gingivaux
Autour des implants, ils peuvent servir à la fois de facteur inflammatoire et de site de colonisation bactérienne, et se sont également révélés être un facteur dans le développement de la maladie17.
diagnostic
Le processus diagnostique comprend un examen clinique et radiographique. L'examen clinique comprend la mesure des poches autour de l'implant, tandis que l'examen radiographique comprend une radiographie périapicale.
Utilisés pour évaluer la hauteur osseuse, ces tests sont importants non seulement pour le diagnostic, mais aussi pour surveiller la santé des tissus entourant l'implant.
Une radiographie diagnostique doit être prise le jour de la pose de l'implant, puis le jour de la mise en charge. Cette seconde radiographie servira de référence pour le suivi du support osseux de l'implant.
Parce qu'elle est réalisée après le processus initial de remodelage physiologique qui se produit autour de l'implant12, 28. L'hypothèse courante est que la perte osseuse qui se produit après le processus initial de remodelage physiologique
Le remodelage physiologique est le résultat d'une infection bactérienne. 6. Lors des examens de suivi, lorsque le clinicien constate un saignement et/ou une augmentation de la profondeur des poches autour de l'implant,
Prenez une radiographie pour vérifier la perte osseuse autour.
Traitement
Il est important de rappeler qu’à ce jour, il n’existe aucun traitement qui constitue une norme de soins dans les cas de péri-implantite, et que des études supplémentaires sont nécessaires pour obtenir une réponse plus claire.
L'efficacité des différents traitements contre cette maladie souligne l'importance de la prévention. La mucite péri-implantaire et la péri-implantite sont des maladies distinctes qui nécessitent un traitement différent.
La mucite péri-implantaire, contrairement à la péri-implantite, est une maladie réversible5,29 et peut généralement être traitée à l’aide d’une technique non chirurgicale12.
Ce traitement comprend l'élimination mécanique quotidienne de la plaque dentaire et un entretien par un hygiéniste. Contrairement à la mucite péri-implantaire, le traitement non chirurgical de la péri-implantite
La plupart des études ont montré qu'il était inefficace 12,30,31 et nécessite donc une intervention chirurgicale utilisant un lambeau de levage (débridement chirurgical à lambeau ouvert - OFD).
Le traitement chirurgical comprend généralement l'ablation du tissu de granulation et le nettoyage de la surface de l'implant. Une résection osseuse ou une régénération du défaut osseux peut également être réalisée.
La décision d’effectuer un traitement restaurateur ou régénératif dépend des exigences esthétiques du site, de la morphologie du défaut osseux et de la présence ou de l’absence de dents ou d’implants adjacents.
Le traitement chirurgical s'est avéré plus efficace que le traitement non chirurgical. L'efficacité du traitement non chirurgical peut être limitée en raison de l'anatomie de l'implant et/ou de sa structure et de sa restauration12.
Traitement non chirurgical par jet de gel de chlorhexidine – premiers résultats encourageants
Dans une étude récente, l’efficacité du dispositif à jet en combinaison avec le gel de chlorhexidine dans le traitement des lésions péri-implantaires a été examinée32.
40 patients ont été testés et divisés en un groupe témoin qui a reçu une séance d'entretien, de formation et de suivi et un groupe expérimental qui a également reçu un appareil à jet.
En association avec un gel de chlorhexidine pour un usage quotidien à domicile. Après 3 mois, l'état a été réévalué. Lors de cette réévaluation,
Une diminution plus significative de la profondeur des poches a été constatée dans le groupe expérimental qui utilisait le dispositif à jet en combinaison avec le gel de chlorhexidine.
Les changements dans la profondeur des poches peuvent être observés dans les graphiques 1 + 2. De plus, une diminution significative du nombre de sites de saignement a été constatée dans le groupe expérimental qui a utilisé
Comparativement au groupe témoin, le dispositif à jet, associé au gel de chlorhexidine, a été utilisé. Il est important de noter que le jet n'est pas destiné à remplacer une hygiène bucco-dentaire rigoureuse et appropriée.
Mais pour ajouter un élément supplémentaire de désinfection du site, il est également possible que, tout comme le jet a contribué au traitement des lésions autour des implants, il joue également un rôle dans la prévention de ces lésions.
Il serait donc recommandé de l'ajouter au panier d'appareils fournis aux patients afin de réaliser un bon entretien des implants.
Graphique 1 Évolution de la profondeur moyenne des poches après 3 mois :
(extrait de l'article, Levin L, Frankenthal S, Joseph L Rozitsky D, Levi G, Machtei EE. Jet d'eau avec gel de chlorhexidine ajouté pour le traitement non chirurgical de la péri-implantite Quintessence Int. 2014;45: Sous presse)
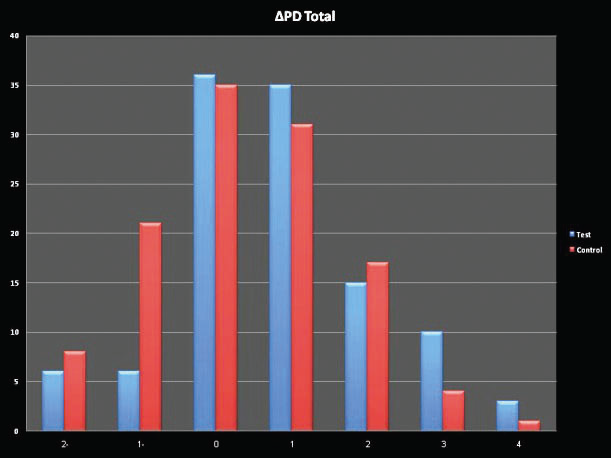
Graphique 2 Évolution de la poche la plus profonde autour de l'implant après 3 mois :
(Extrait de l'article, Levin L, Frankenthal S, Joseph L Rozitsky D, Levi G, Machtei EE. Jet d'eau avec traitement non chirurgical complémentaire de la péri-. Gel de chlorhexidine pour l'implantite. Quintessence Int 2014;45: Sous presse)

Jusqu'à présent, aucun traitement efficace n'a été trouvé contre la péri-implantite. En attendant qu'un traitement spécifique soit efficace, il est nécessaire de se concentrer sur la prévention, car c'est le traitement le plus efficace aujourd'hui.
Avant de pouvoir poser des implants, nous devons d’abord réaliser un traitement parodontal complet tout en traitant les facteurs de risque systémiques de la maladie et atteindre un état où il n’y a pas de maladie active dans la cavité buccale.
Il est également nécessaire d’informer le patient sur le risque lié au traitement implantaire et sur la manière dont il peut être réduit, tout en maintenant une hygiène bucco-dentaire stricte et en réduisant les facteurs de risque systémiques.
comme le tabagisme et le contrôle du diabète. Il est important de souligner l'importance d'un suivi régulier et rigoureux pour la réussite à long terme du traitement. Comme pour toute maladie inflammatoire,
Une détection précoce de la maladie permettra une intervention rapide dès les premiers stades et un meilleur pronostic. À cette fin, une surveillance régulière des implants est nécessaire dans le cadre de l'évaluation et de l'entretien parodontaux.33.
Extrait du magazine n° 19 du 14 octobre, pages 46-47, voir RÉFÉRENCES page 48
Type d'essai clinique, article de revue, essai contrôlé randomisé, étude comparative Résumé
Objectifs : L’objectif de cet essai clinique en double aveugle était d’évaluer la
L’efficacité et les effets secondaires de deux types différents de bains de bouche.
Méthode et matériel : Quatre-vingt-dix sujets atteints de gingivite ou de parodontite légère
la parodontite a été divisée au hasard en trois groupes : Chlorhexamed 0,1% 1 groupe chlorhexidine.
Groupe 2, Hexoral 0.1%, hexidine et groupe 3, une préparation placebo pour le contrôle.
Les sujets ont reçu des instructions sur l'utilisation du bain de bouche. Au début, puis après deux et quatre semaines, les indicateurs suivants ont été mesurés :
Plaque interdentaire API, indice de saignement BI, indice de communauté parodontale pour le besoin de traitements, indice gingival
Indice de changement de couleur GI et DI L'analyse statistique a été réalisée à l'aide du test de Kruskal-Wallis, du test exact de Fisher et du test de Wilcoxon.
Résultats : Dans le groupe API, la moyenne 1 s’est améliorée de manière significative (P>0,001) après quatre semaines.
L'IB moyen a diminué de manière significative, tout comme l'IG. L'IB moyen, l'API et l'IG ont diminué de manière significative dans le groupe 2, et il est également apparu
Réduction statistiquement significative de l'IG. Dans le groupe 3, après quatre semaines, des améliorations significatives ont été enregistrées.
des valeurs moyennes de tous les paramètres. En comparant le groupe 3 aux groupes 1 et 2, la différence de diminution
L'API était statistiquement significative (p < 0,002). Aucune différence statistique n'a été observée lors de la comparaison des groupes.
1 et 2 - Concernant les résultats améliorés de BI et GI, aucune différence statistique significative n'a été constatée dans l'efficacité des trois
Préparations. Les trois groupes ont montré une augmentation de l'ID après quatre semaines. Une comparaison directe entre le groupe 1 et le groupe 2 a été réalisée.
Pour le 2-, la différence dans l’augmentation de la décoloration des dents était statistiquement significative (P = 0,0035, aucune différence n’a été trouvée).
Différence statistiquement significative dans les taux moyens de changement de couleur comparés entre les groupes 2 et 3.
Conclusion : Cet essai clinique en double aveugle a démontré qu’Hexoral (hexétidine) est une bonne alternative au bain de bouche.
(Chlorhexamed (Chlorhexidine), et provoque également moins de décoloration des dents.